Die Forschungsgruppe Bioprogrammierbare Materialien erforscht ein junges multidisziplinäres Feld, das synthetische Biologie und Biomaterialien kombiniert. Im Mittelpunkt steht die Entwicklung von Materialien mit genetisch programmierten Funktionalitäten, die für Biosensorik geeignet sowie in der Lage sind, auf Stimuli hin Medikamente langfristig freizusetzen und das Zellverhalten zu beeinflussen. Mit Werkzeugen aus der synthetischen Biologie werden Proteine und Mikroben so programmiert, dass sie intelligente und nützliche Funktionen erfüllen. Diese technisierten biologischen Gebilde werden dann in entsprechend entwickelte polymere Matrizen eingearbeitet. Das Ergebnis sind Kompositmaterialien mit sehr vielseitigen Funktionalitäten, einer großen Bandbreite an Steuerbarkeit und in situ-Kontrollmöglichkeiten.
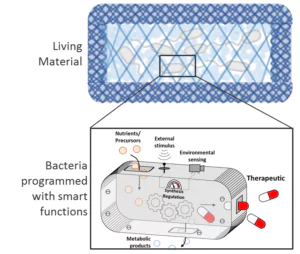
Bakterien werden mit intelligenten Funktionen versehen, beispielsweise für Anwendungen in den Bereichen Biosensorik und Wirkstofftransport

Mitarbeiter/innen





Forschung
In der Gruppe Bioprogrammierbare Materialien kombinieren wir genetisch programmierte lebende Organismen wie Bakterien mit polymeren Matrices wie Hydrogelen, um intelligente Verbundwerkstoffe, so genannte Engineered Living Materials (ELMs), herzustellen. Durch innovative Ansätze bei den lebenden wie bei den nicht-lebenden Materialien sind unsere ELMs für ganze eine Reihe von biomedizinischen Anwendungen wie Biosensorik und Medikamentenabgabe geeignet:
Stimuli-responsive Drug-Sekretion in Bakterien
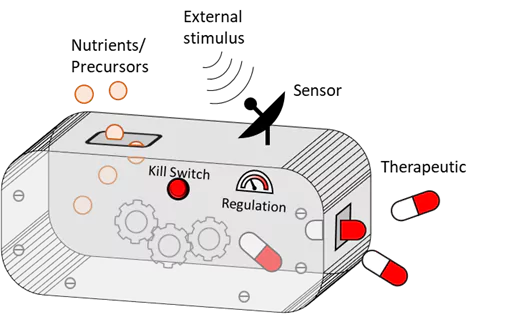
Bakterien sind ein wesentlicher Bestandteil des Mikrobioms des Körpers, wobei mehrere native und probiotische Arten dem Menschen einen natürlichen Gesundheitsschutz verleihen. Bakterien werden auch in der pharmazeutischen Industrie in großem Umfang als Biofabriken zur Herstellung einer Vielzahl von Arzneimitteln eingesetzt. Unsere Forschung vereint diese beiden Merkmale: Wir entwickeln medizinisch relevante Bakterien wie E. coli, Lactobacilli und Corynebacterium, um therapeutische Moleküle direkt im Körper dort zu produzieren und abzusondern, wo sie benötigt werden. Da die Bakterien auf natürliche Weise im Körper gedeihen, kann eine langfristige Freisetzung des Arzneimittels aufrechterhalten werden. Wir designen die Bakterien so, dass sie antimikrobielle, entzündungshemmende und regenerative Medikamente in Form von Peptiden, Proteinen und enzymatisch synthetisierten Biomolekülen zur Behandlung chronischer Krankheiten produzieren und freisetzen.
Patientenprofile und Krankheitsverläufe können sehr unterschiedlich sein. Daher sollte die Aktivität dieser therapeutischen Bakterien so personalisiert und angepasst werden können, dass eine größtmögliche Wirksamkeit sichergestellt ist. Dazu entwickeln wir genetische Module, die die Wirkstofffreisetzung über externe Reize„anschalten“. Stimuli wie Licht, Wärme und kleine Moleküle ermöglichen die Fernsteuerung der Bakterien, und Stimuli wie Biomarker reagieren auf das Fortschreiten der Krankheit und können die Aktivität der Bakterien mittels Autoregulation verändern. Stimuli-responsive genetische Module werden ebenfalls als zusätzliche Ebene der Biosicherheit entwickelt. Damit stellen wir sicher, dass Bakterien nicht außerhalb ihrer vorgesehenen Implantatumgebung überleben. Während viele der von uns verwendeten genetischen Module ursprünglich für E. coli entwickelt wurden, statten wir nun auch probiotische Bakterien wie Laktobazillen und Corynebacterium mit ähnlichen Funktionen aus – eine Herausforderung, die durch die Erweiterung des Spektrums an ELM-fähigen Organismen und Funktionen erhebliche Vorteile verspricht.
Neuste Veröffentlichungen:
- Dhakane, P.; Tadimarri, V. S.; Sankaran, S. Light-Regulated pro-Angiogenic Engineered Living Materials. bioRxiv – https://doi.org/10.1101/2022.10.28.514190.
- Dey, S.; Asensio, M. B.; Kuttae, S. B.; Sankaran, S. Novel Genetic Modules Encoding High-Level Antibiotic-Free Protein Expression in Probiotic Lactobacilli. bioRxiv – https://doi.org/10.1101/2022.08.04.502766.
Hydrogele für die bakterielle Einkapselung und Werkzeuge zum Verständnis des bakteriellen Verhaltens in Gefangenschaft
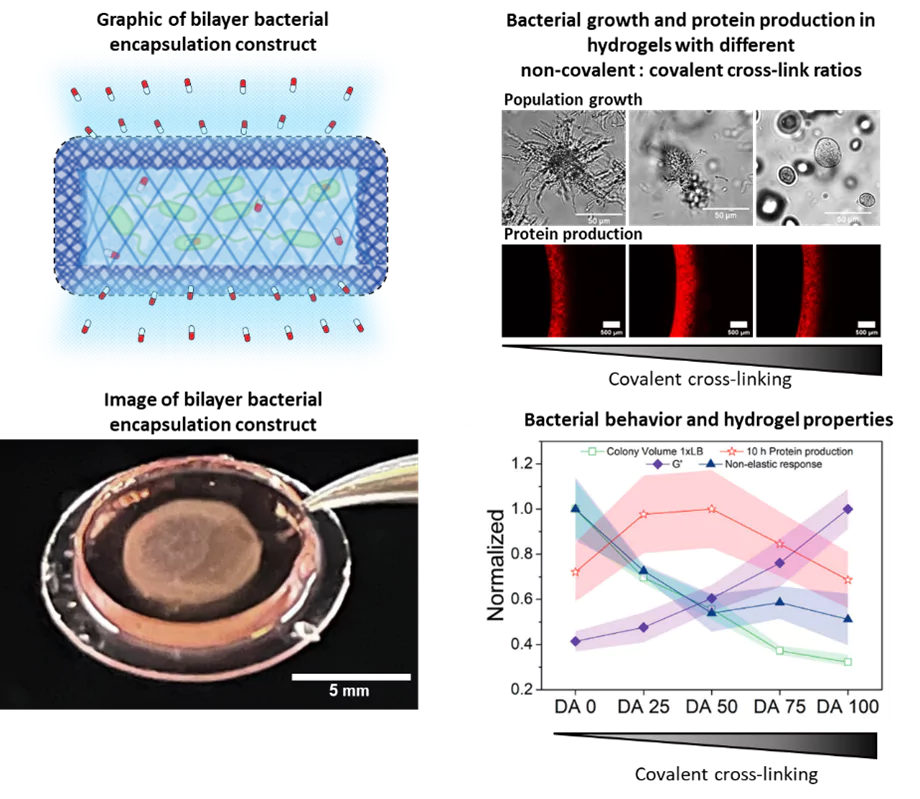
Für die therapeutischen Bakterien zur Behandlung einer Krankheit ist es notwendig, dass sie sich an der Krankheitsstelle ansiedeln und eine ausreichend große Population aufbauen, um wirksame Medikamentendosen bereitzustellen. In Zusammenarbeit mit der Forschungsgruppe Dynamische Biomaterialien entwickeln wir hydrogelbasierte Matrizen, die geeignete Umgebungen für das Wachstum und die Funktion der Bakterien bieten. Diese Hydrogele sind so konzipiert, dass sie die Größe der enthaltenen Bakterienpopulation mechanisch kontrollieren und gleichzeitig deren Funktionalität maximieren. Das Hydrogelnetzwerk ermöglicht die Diffusion von Nährstoffen, Metaboliten und Medikamenten in und aus der Matrix, während es das Entweichen der Bakterien verhindert und Schutz vor Immunzellen bietet. Die Materialkomponente bietet daher eine zusätzliche Ebene der Biosicherheit für den Einsatz von genetisch veränderten Bakterien im Körper.
Im Rahmen dieser Forschung haben wir festgestellt, dass bestimmte mechanische Eigenschaften der Hydrogele das Wachstum und den Stoffwechsel der enthaltenen Bakterien beeinflussen, ähnlich wie es bei natürlichen Biofilmen der Fall ist. Dies wirkt sich wiederum auf die Leistungsfähigkeit der Bakterien in Bezug auf die Reaktion auf Stimuli und die Produktion von Medikamenten aus. Daher untersuchen wir das Verhalten der Bakterien in den eingeschränkten Bedingungen der Hydrogele, deren mechanische Eigenschaften wir steuern können. Dabei erkennen wir das Zusammenspiel zwischen dem kollektiven Verhalten der Bakterien und den sie umgebenden mechanischen Kräften. Neben der Optimierung der Leistungsfähigkeit der von uns entwickelten lebenden Materialien dient dies auch als künstliche Plattform für Biofilme, um grundlegende Erkenntnisse über das mögliche Verhalten von Bakterien in verschiedenen Bereichen natürlicher Biofilme zu gewinnen. Zur Bestimmung des Wachstums und des Stoffwechselverhaltens der Bakterien im Laufe der Zeit nutzen wir Mikroskopie sowie biochemische und genetische Tests.
Neuste Veröffentlichungen:
- Bhusari, S.; Sankaran, S.; del Campo, A. Regulating Bacterial Behavior within Hydrogels of Tunable Viscoelasticity. Advanced Science 2022, 9 (17), 2106026. https://doi.org/10.1002/advs.202106026.
- Bhusari, S.; Kim, J.; Polizzi, K.; Sankaran, S.; Campo, A. del. Encapsulation of Bacteria in Bilayer Pluronic Thin Film Hydrogels: A Safe Format for Engineered Living Materials. bioRxiv – https://doi.org/10.1101/2022.09.29.510162.
Kooperationen:
Diese Forschungsanstrengungen sind auch Teil mehrerer Kooperationen innerhalb zweier Konsortien – (i) Leibniz Wissenschaftscampus – Living Therapeutic Materials (LSC LifeMat) und (ii) Sonderforschungsbereich on Physikalische Modellierung von Nichtgleichgewichtsprozessen in biologischen Systemen (SFB 1027).
Finanzierung:


Publikationen
Dey, Sourik | Sankaran, Shrikrishnan
DOI:
Recent advances in engineered bacterial therapeutics underscore their potential in treating diseases via targeted, live interventions. Despite their promising performance in early clinical phases, no engineered therapeutic bacteria have yet received approval, primarily due to challenges in proving efficacy while ensuring biosafety. Material science innovations, particularly the encapsulation of bacteria within hydrogels, present a promising avenue to enhance bacterial survival, efficacy, and safety in therapeutic applications. This review discusses this interdisciplinary approach to develop living therapeutic materials. Hydrogels not only safeguard the bacteria from harsh physiological conditions but also enable controlled therapeutic release and prevent unintended bacterial dissemination. The strategic use of encapsulation materials could redefine the delivery and functionality of engineered bacterial therapeutics, facilitating their clinical translation.
Korkmaz, Nuriye | Himawan, Sandiego | Usman, Muhammed | Baik, Seungyun | Kim, Minyoung
DOI:
In this study, fd viruses are genetically modified to display seven cropped versions (H, HG, HGF, HGFA, HGFAN, HGFANV and HGFANVA) of the previously identified Cu(II) specific peptide (HGFANVA). Atomic force microscopy (AFM) imaging reveals the typical filamentous structures of recombinant phages with thicknesses of ≈2–5 nm in dry state. Scanning electron microscopy (SEM) imaging shows that HGFANVA viruses form larger elongated assemblies than H viruses that are deposited with a mineral layer after Cu(II) treatment. C and N peaks are detected for virus samples through Energy dispersive X-ray spectroscopy (EDX) analyses confirming the presence of phage organic material. Cu peak is only detected for engineered viruses after Cu(II) exposure. Enzyme-linked immunosorbent assay (ELISA) analyses show the selective Cu(II) binding of engineered phages. Agarose gel electrophoresis (AGE) and zeta potential analyses reveal negative surface charges of engineered viral constructs. Positively charged Cytopore beads are coated with bacteriophages and used for Cu(II) ion sorption studies. ICP-MS analyses clearly show the improved Cu(II) binding of engineered viruses with respect to wild-type fd phages. Such bottom-up constructed, genetically engineered virus-based biomaterials may be applied in bioremediation studies targeting metal species from environmental samples.
Dey, Sourik | Sankaran, Shrikrishnan
DOI:
Zhu et al. introduce MELG (materials engineered by living grafting), combining engineered microbes with non-living scaffolds for functional protein regeneration within. These MELGs can be used for long-term controlled release, enzyme-mediated biocatalysis, and DNA purification. This approach offers enhanced functionality and durability in bioactive materials compared to traditional non-living counterparts.
Dey, Sourik | Seyfert, Carsten E. | Fink-Straube, Claudia | Kany, Andreas Martin | Müller, Rolf | Sankaran, Shrikrishnan
DOI:
Peptide drugs have seen rapid advancement in biopharmaceutical development, with over 80 candidates approved
globally. Despite their therapeutic potential, the clinical translation of peptide drugs is hampered by challenges
in production yields and stability. Engineered bacterial therapeutics is a unique approach being explored to overcome
these issues by using bacteria to produce and deliver therapeutic compounds at the body site of use. A key advan‑
tage of this technology is the possibility to control drug delivery within the body in real time using genetic switches.
However, the performance of such genetic switches suffers when used to control drugs that require post‑translational
modifications or are toxic to the host. In this study, these challenges were experienced when attempting to establish
a thermal switch for the production of a ribosomally synthesized and post‑translationally modified peptide antibiotic,
darobactin, in probiotic E. coli. These challenges were overcome by developing a thermo‑amplifier circuit that com‑
bined the thermal switch with a T7 RNA Polymerase. Due to the orthogonality of the Polymerase, this strategy
overcame limitations imposed by the host transcriptional machinery. This circuit enabled production of pathogen‑
inhibitory levels of darobactin at 40 °C while maintaining leakiness below the detection limit at 37 °C. Furthermore,
the thermo‑amplifier circuit sustained gene expression beyond the thermal induction duration such that with only
2 h of induction, the bacteria were able to produce pathogen‑inhibitory levels of darobactin. This performance
was maintained even in physiologically relevant simulated conditions of the intestines that include bile salts and low
nutrient levels
Bhusari, Shardul | Kim, Juhyun | Polizzi, Karen | Sankaran, Shrikrishnan | del Campo, Aránzazu
DOI:
In engineered living materials (ELMs) non-living matrices encapsulate microorganisms to acquire capabilities like sensing or biosynthesis. The confinement of the organisms to the matrix and the prevention of overgrowth and escape during the lifetime of the material is necessary for the application of ELMs into real devices. In this study, a bilayer thin film hydrogel of Pluronic F127 and Pluronic F127 acrylate polymers supported on a solid substrate is introduced. The inner hydrogel layer contains genetically engineered bacteria and supports their growth, while the outer layer acts as an envelope and does not allow leakage of the living organisms outside of the film for at least 15 days. Due to the flat and transparent nature of the construct, the thin layer is suited for microscopy and spectroscopy-based analyses. The composition and properties of the inner and outer layer are adjusted independently to fulfil viability and confinement requirements. We demonstrate that bacterial growth and light-induced protein production are possible in the inner layer and their extent is influenced by the crosslinking degree of the used hydrogel. Bacteria inside the hydrogel are viable long term, they can act as lactate-sensors and remain active after storage in phosphate buffer at room temperature for at least 3 weeks. The versatility of bilayer bacteria thin-films is attractive for fundamental studies and for the development of application-oriented ELMs.
Basaran, Selim | Dey, Sourik | Bhusari, Shardul | Sankaran, Shrikrishnan | Kraus, Tobias
DOI:
Engineered living materials (ELMs) encapsulate microorganisms within polymeric matrices for biosensing, drug delivery, capturing viruses, and bioremediation. It is often desirable to control their function remotely and in real time and so the microorganisms are often genetically engineered to respond to external stimuli. Here, we combine thermogenetically engineered microorganisms with inorganic nanostructures to sensitize an ELM to near infrared light. For this, we use plasmonic gold nanorods (AuNR) that have a strong absorption maximum at 808 nm, a wavelength where human tissue is relatively transparent. These are combined with Pluronic-based hydrogel to generate a nanocomposite gel that can convert incident near infrared light into heat locally. We perform transient temperature measurements and find a photothermal conversion efficiency of 47 %. Steady-state temperature profiles from local photothermal heating are quantified using infrared photothermal imaging and correlated with measurements inside the gel to reconstruct spatial temperature profiles. Bilayer geometries are used to combine AuNR and bacteria-containing gel layers to mimic core-shell ELMs. The thermoplasmonic heating of an AuNR-containing hydrogel layer that is exposed to infrared light diffuses to the separate but connected hydrogel layer with bacteria and stimulates them to produce a fluorescent protein. By tuning the intensity of the incident light, it is possible to activate either the entire bacterial population or only a localized region.
Yanamandra, Archana K. | Bhusari, Shardul | del Campo, Aránzazu | Sankaran, Shrikrishnan | Qu, Bin
DOI:
In living therapeutic materials (LTMs), organisms genetically programmed to produce and deliver drugs are encapsulated in porous matrices acting as physical barriers between the therapeutic organisms and the host cells. LTMs consisting of engineered E. coli encapsulated in Pluronic F127-based hydrogels have been frequently used in LTM designs but their immunogenicity has not been tested. In this study, we investigate the response of human peripheral blood mononuclear cells (PBMCs) exposed to this bacteria/hydrogel combination. The release of inflammation-related cytokines and cytotoxic proteins and the subsets of natural killer cells and T cells were examined. Encapsulation of the bacteria in hydrogels considerably lowers their immunogenicity. ClearColi, an endotoxin-free variant of E. coli, did not polarize NK cells into the more cytolytic CD16dim subset as E. coli. Our results demonstrate that ClearColi-encapsulated hydrogels generate low immunogenic response and are suitable candidates for the development of LTMs for in vivo testing to assess a potential clinical use. Nevertheless, we observed a stronger immune response (elevated levels of IFNγ, IL-6 and cytotoxic proteins) in pro-inflammatory PBMCs characterized by a high spontaneous release of IL-2. This highlights the need to identify recipients who have a higher likelihood of experiencing undesired immune responses to LTMs with IL-2 serving as a potential predictive marker. Additionally, including anti-inflammatory measures in living therapeutic material designs could be beneficial for such recipients.
Riedel, Florian | Puertas Bartolomé, María | Teruel Enrico, Lara Luana | Fink-Straube, Claudia | Nguyen Dong, Cao | Gherlone, Fabio | Huang, Ying | Valiante, Vito | del Campo, Aránzazu | Sankaran, Shrikrishnan
DOI:
Microbial biofactories allow the upscaled production of high-value compounds in biotechnological processes. This is particularly advantageous for compounds like flavonoids that promote better health through their antioxidant, antibacterial, anticancer and other beneficial effects but are only produced in small quantities in their natural plant-based hosts. Bacteria like E. coli have been genetically modified with enzyme cascades to produce flavonoids like naringenin and pinocembrin from coumaric or cinnamic acid. Despite advancements in yield optimization, the production of these compounds still involves high costs associated with their biosynthesis, purification, storage and transport. An alternative production strategy could involve the direct delivery of the microbial biofactories to the body. In such a strategy, ensuring biocontainment of the engineered microbes in the body and controlling production rates are major challenges. In this study, these two aspects are addressed by developing engineered living materials (ELMs) consisting of probiotic microbial biofactories encapsulated in biocompatible hydrogels. Engineered probiotic E. coli Nissle 1917 able to efficiently convert cinnamic acid into pinocembrin were encapsulated in poly(vinyl alcohol)-based hydrogels. The biofactories are contained in the hydrogels for a month and remain metabolically active during this time. Control over production levels is achieved by the containment inside the material, which regulates bacteria growth, and by the amount of cinnamic acid in the medium.
Blanch-Asensio, Marc | Dey, Sourik | Sankaran, Shrikrishnan
DOI:
Lactobacilli are gram-positive bacteria that are growing in importance for the healthcare industry and genetically engineering them as living therapeutics is highly sought after. However, progress in this field is hindered since most strains are difficult to genetically manipulate, partly due to their complex and thick cell walls limiting our capability to transform them with exogenous DNA. To overcome this, large amounts of DNA (>1 µg) are normally required to successfully transform these bacteria. An intermediate host, like E. coli, is often used to amplify recombinant DNA to such amounts although this approach poses unwanted drawbacks such as an increase in plasmid size, different methylation patterns and the limitation of introducing only genes compatible with the intermediate host. In this work, we have developed a direct cloning method based on in-vitro assembly and PCR amplification to yield recombinant DNA in significant quantities for successful transformation in L. plantarum WCFS1. The advantage of this method is demonstrated in terms of shorter experimental duration and the possibility to introduce a gene incompatible with E. coli into L. plantarum WCFS1.




