Die Forschungsgruppe Bioprogrammierbare Materialien erforscht ein junges multidisziplinäres Feld, das synthetische Biologie und Biomaterialien kombiniert. Im Mittelpunkt steht die Entwicklung von Materialien mit genetisch programmierten Funktionalitäten, die für Biosensorik geeignet sowie in der Lage sind, auf Stimuli hin Medikamente langfristig freizusetzen und das Zellverhalten zu beeinflussen. Mit Werkzeugen aus der synthetischen Biologie werden Proteine und Mikroben so programmiert, dass sie intelligente und nützliche Funktionen erfüllen. Diese technisierten biologischen Gebilde werden dann in entsprechend entwickelte polymere Matrizen eingearbeitet. Das Ergebnis sind Kompositmaterialien mit sehr vielseitigen Funktionalitäten, einer großen Bandbreite an Steuerbarkeit und in situ-Kontrollmöglichkeiten.
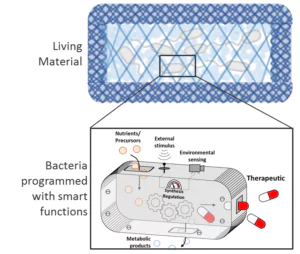
Bakterien werden mit intelligenten Funktionen versehen, beispielsweise für Anwendungen in den Bereichen Biosensorik und Wirkstofftransport

Mitarbeiter/innen





Forschung
In der Gruppe Bioprogrammierbare Materialien kombinieren wir genetisch programmierte lebende Organismen wie Bakterien mit polymeren Matrices wie Hydrogelen, um intelligente Verbundwerkstoffe, so genannte Engineered Living Materials (ELMs), herzustellen. Durch innovative Ansätze bei den lebenden wie bei den nicht-lebenden Materialien sind unsere ELMs für ganze eine Reihe von biomedizinischen Anwendungen wie Biosensorik und Medikamentenabgabe geeignet:
Stimuli-responsive Drug-Sekretion in Bakterien
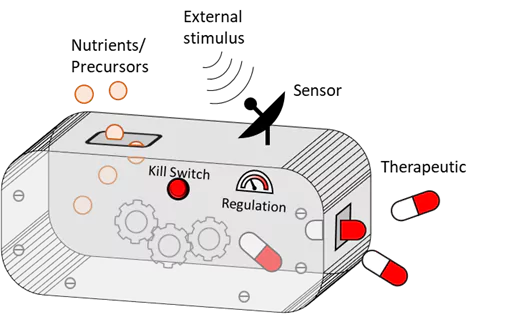
Bakterien sind ein wesentlicher Bestandteil des Mikrobioms des Körpers, wobei mehrere native und probiotische Arten dem Menschen einen natürlichen Gesundheitsschutz verleihen. Bakterien werden auch in der pharmazeutischen Industrie in großem Umfang als Biofabriken zur Herstellung einer Vielzahl von Arzneimitteln eingesetzt. Unsere Forschung vereint diese beiden Merkmale: Wir entwickeln medizinisch relevante Bakterien wie E. coli, Lactobacilli und Corynebacterium, um therapeutische Moleküle direkt im Körper dort zu produzieren und abzusondern, wo sie benötigt werden. Da die Bakterien auf natürliche Weise im Körper gedeihen, kann eine langfristige Freisetzung des Arzneimittels aufrechterhalten werden. Wir designen die Bakterien so, dass sie antimikrobielle, entzündungshemmende und regenerative Medikamente in Form von Peptiden, Proteinen und enzymatisch synthetisierten Biomolekülen zur Behandlung chronischer Krankheiten produzieren und freisetzen.
Patientenprofile und Krankheitsverläufe können sehr unterschiedlich sein. Daher sollte die Aktivität dieser therapeutischen Bakterien so personalisiert und angepasst werden können, dass eine größtmögliche Wirksamkeit sichergestellt ist. Dazu entwickeln wir genetische Module, die die Wirkstofffreisetzung über externe Reize„anschalten“. Stimuli wie Licht, Wärme und kleine Moleküle ermöglichen die Fernsteuerung der Bakterien, und Stimuli wie Biomarker reagieren auf das Fortschreiten der Krankheit und können die Aktivität der Bakterien mittels Autoregulation verändern. Stimuli-responsive genetische Module werden ebenfalls als zusätzliche Ebene der Biosicherheit entwickelt. Damit stellen wir sicher, dass Bakterien nicht außerhalb ihrer vorgesehenen Implantatumgebung überleben. Während viele der von uns verwendeten genetischen Module ursprünglich für E. coli entwickelt wurden, statten wir nun auch probiotische Bakterien wie Laktobazillen und Corynebacterium mit ähnlichen Funktionen aus – eine Herausforderung, die durch die Erweiterung des Spektrums an ELM-fähigen Organismen und Funktionen erhebliche Vorteile verspricht.
Neuste Veröffentlichungen:
- Dhakane, P.; Tadimarri, V. S.; Sankaran, S. Light-Regulated pro-Angiogenic Engineered Living Materials. bioRxiv – https://doi.org/10.1101/2022.10.28.514190.
- Dey, S.; Asensio, M. B.; Kuttae, S. B.; Sankaran, S. Novel Genetic Modules Encoding High-Level Antibiotic-Free Protein Expression in Probiotic Lactobacilli. bioRxiv – https://doi.org/10.1101/2022.08.04.502766.
Hydrogele für die bakterielle Einkapselung und Werkzeuge zum Verständnis des bakteriellen Verhaltens in Gefangenschaft
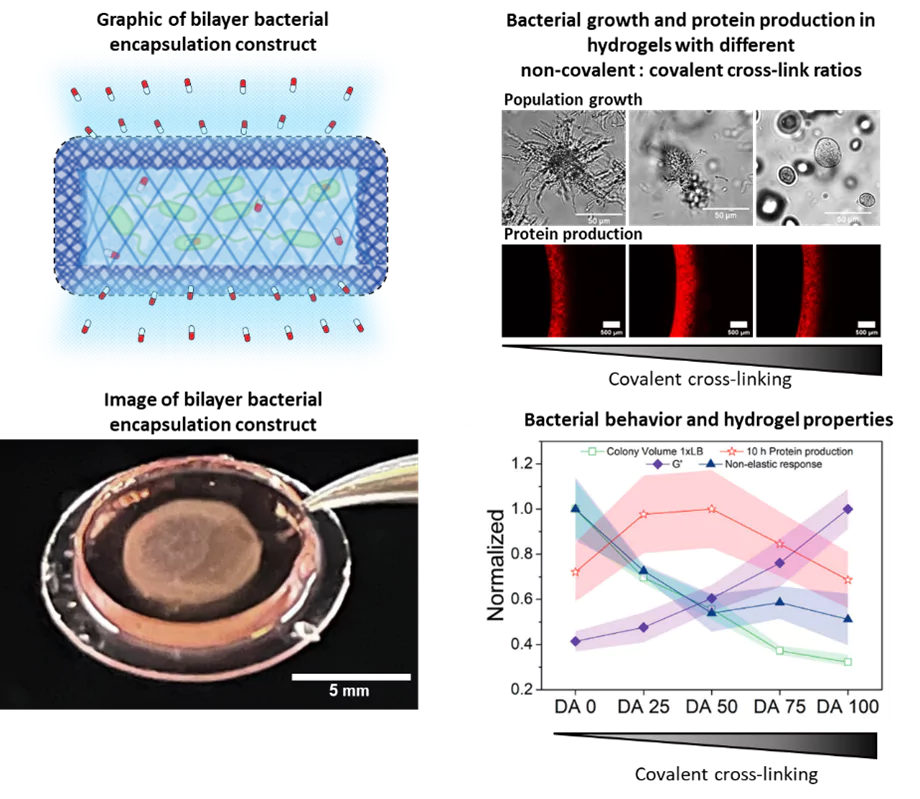
Für die therapeutischen Bakterien zur Behandlung einer Krankheit ist es notwendig, dass sie sich an der Krankheitsstelle ansiedeln und eine ausreichend große Population aufbauen, um wirksame Medikamentendosen bereitzustellen. In Zusammenarbeit mit der Forschungsgruppe Dynamische Biomaterialien entwickeln wir hydrogelbasierte Matrizen, die geeignete Umgebungen für das Wachstum und die Funktion der Bakterien bieten. Diese Hydrogele sind so konzipiert, dass sie die Größe der enthaltenen Bakterienpopulation mechanisch kontrollieren und gleichzeitig deren Funktionalität maximieren. Das Hydrogelnetzwerk ermöglicht die Diffusion von Nährstoffen, Metaboliten und Medikamenten in und aus der Matrix, während es das Entweichen der Bakterien verhindert und Schutz vor Immunzellen bietet. Die Materialkomponente bietet daher eine zusätzliche Ebene der Biosicherheit für den Einsatz von genetisch veränderten Bakterien im Körper.
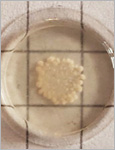
Im Rahmen dieser Forschung haben wir festgestellt, dass bestimmte mechanische Eigenschaften der Hydrogele das Wachstum und den Stoffwechsel der enthaltenen Bakterien beeinflussen, ähnlich wie es bei natürlichen Biofilmen der Fall ist. Dies wirkt sich wiederum auf die Leistungsfähigkeit der Bakterien in Bezug auf die Reaktion auf Stimuli und die Produktion von Medikamenten aus. Daher untersuchen wir das Verhalten der Bakterien in den eingeschränkten Bedingungen der Hydrogele, deren mechanische Eigenschaften wir steuern können. Dabei erkennen wir das Zusammenspiel zwischen dem kollektiven Verhalten der Bakterien und den sie umgebenden mechanischen Kräften. Neben der Optimierung der Leistungsfähigkeit der von uns entwickelten lebenden Materialien dient dies auch als künstliche Plattform für Biofilme, um grundlegende Erkenntnisse über das mögliche Verhalten von Bakterien in verschiedenen Bereichen natürlicher Biofilme zu gewinnen. Zur Bestimmung des Wachstums und des Stoffwechselverhaltens der Bakterien im Laufe der Zeit nutzen wir Mikroskopie sowie biochemische und genetische Tests.
Neuste Veröffentlichungen:
- Bhusari, S.; Sankaran, S.; del Campo, A. Regulating Bacterial Behavior within Hydrogels of Tunable Viscoelasticity. Advanced Science 2022, 9 (17), 2106026. https://doi.org/10.1002/advs.202106026.
- Bhusari, S.; Kim, J.; Polizzi, K.; Sankaran, S.; Campo, A. del. Encapsulation of Bacteria in Bilayer Pluronic Thin Film Hydrogels: A Safe Format for Engineered Living Materials. bioRxiv – https://doi.org/10.1101/2022.09.29.510162.
Kooperationen:
Diese Forschungsanstrengungen sind auch Teil mehrerer Kooperationen innerhalb zweier Konsortien – (i) Leibniz Wissenschaftscampus – Living Therapeutic Materials (LSC LifeMat) und (ii) Sonderforschungsbereich on Physikalische Modellierung von Nichtgleichgewichtsprozessen in biologischen Systemen (SFB 1027).
Finanzierung:


Publikationen

Dey, Sourik | Blanch-Asensio, Marc | Kuttae, Sanjana Balaji | Sankaran, Shrikrishnan
DOI:
Lactobacilli are ubiquitous in nature, often beneficially associated with animals as commensals and probiotics, and are extensively used in food fermentation. Due to this close-knit association, there is considerable interest to engineer them for healthcare applications in both humans and animals, for which high-performance and versatile genetic parts are greatly desired. For the first time, we describe two genetic modules in Lactiplantibacillus plantarum that achieve high-level gene expression using plasmids that can be retained without antibiotics, bacteriocins or genomic manipulations. These include (i) a promoter, PtlpA, from a phylogenetically distant bacterium, Salmonella typhimurium, which drives up to 5-fold higher level of gene expression compared to previously reported promoters and (ii) multiple toxin-antitoxin systems as a self-contained and easy-to-implement plasmid retention strategy that facilitates the engineering of tuneable transient genetically modified organisms. These modules and the fundamental factors underlying their functionality that are described in this work will greatly contribute to expanding the genetic programmability of lactobacilli for healthcare applications.
Riedel, Florian | Puertas Bartolomé, María | Teruel Enrico, Lara Luana | Fink-Straube, Claudia | Nguyen Dong, Cao | Gherlone, Fabio | Huang, Ying | Valiante, Vito | del Campo, Aránzazu | Sankaran, Shrikrishnan
DOI:
Microbial biofactories allow the upscaled production of high-value compounds in biotechnological processes. This is particularly advantageous for compounds like flavonoids that promote better health through their antioxidant, antibacterial, anticancer and other beneficial effects but are only produced in small quantities in their natural plant-based hosts. Bacteria like E. coli have been genetically modified with enzyme cascades to produce flavonoids like naringenin and pinocembrin from coumaric or cinnamic acid. Despite advancements in yield optimization, the production of these compounds still involves high costs associated with their biosynthesis, purification, storage and transport. An alternative production strategy could involve the direct delivery of the microbial biofactories to the body. In such a strategy, ensuring biocontainment of the engineered microbes in the body and controlling production rates are major challenges. In this study, these two aspects are addressed by developing engineered living materials (ELMs) consisting of probiotic microbial biofactories encapsulated in biocompatible hydrogels. Engineered probiotic E. coli Nissle 1917 able to efficiently convert cinnamic acid into pinocembrin were encapsulated in poly(vinyl alcohol)-based hydrogels. The biofactories are contained in the hydrogels for a month and remain metabolically active during this time. Control over production levels is achieved by the containment inside the material, which regulates bacteria growth, and by the amount of cinnamic acid in the medium.

Bhusari, Shardul | Sankaran, Shrikrishnan | del Campo, Aránzazu
DOI:
Engineered living materials (ELMs) are a new class of materials in which living organism incorporated into diffusive matrices uptake a fundamental role in material's composition and function. Understanding how the spatial confinement in 3D can regulate the behavior of the embedded cells is crucial to design and predict ELM's function, minimize their environmental impact and facilitate their translation into applied materials. This study investigates the growth and metabolic activity of bacteria within an associative hydrogel network (Pluronic-based) with mechanical properties that can be tuned by introducing a variable degree of acrylate crosslinks. Individual bacteria distributed in the hydrogel matrix at low density form functional colonies whose size is controlled by the extent of permanent crosslinks. With increasing stiffness and elastic response to deformation of the matrix, a decrease in colony volumes and an increase in their sphericity are observed. Protein production follows a different pattern with higher production yields occurring in networks with intermediate permanent crosslinking degrees. These results demonstrate that matrix design can be used to control and regulate the composition and function of ELMs containing microorganisms. Interestingly, design parameters for matrices to regulate bacteria behavior show similarities to those elucidated for 3D culture of mammalian cells.
Rodrigo-Navarro, Aleixandre | Sankaran, Shrikrishnan | Dalby, Matthew J. | del Campo, Aránzazu | Salmeron-Sanchez, Manuel
DOI:
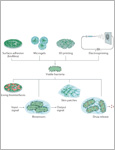
Biomaterials have evolved from inert materials that lack interaction with the body to biologically active, instructive materials that host and provide signals to surrounding cells and tissues. Engineered living materials contain living cells (responsive function) and polymeric matrices (scaffolding function) and, thus, can be designed as active and response biomaterials. In this Review, we discuss engineered living materials that incorporate microorganisms as the living, bioactive component. Microorganisms can provide complex responses to environmental stimuli, and they can be genetically engineered to allow user control over responses and integration of numerous inputs. The engineered microorganisms can either generate their own matrix, such as in biofilms, or they can be incorporated in matrices using various technologies, such as coating, 3D printing, spinning and microencapsulation. We highlight biomedical applications of such engineered living materials, including biosensing, wound healing, stem-cell-based tissue engineering and drug delivery, and provide an outlook to the challenges and future applications of engineered living materials.




