Building Immunity from the Bottom Up
Die Emmy-Noether-Nachwuchsgruppe Immuno Materials entwickelt neue zellbasierte, synthetische Ansätze, um Immunreaktionen zu regulieren und zu untersuchen. Durch den Einsatz von Modellmembransystemen und in-vitro-Rekonstitutionsansätzen, inspiriert von der Bottom-up-Synthetischen Biologie, konstruieren wir kontrollierte zelluläre Umgebungen, die Immunreaktionen in T-Zellen und Krebszellen auslösen. Mit diesem Ansatz untersuchen wir, wie biophysikalische und biochemische Signale die Kommunikation zwischen Krebs- und Immunzellen steuern, und nutzen dieses Wissen, um neuartige Immuntherapien der nächsten Generation zu verbessern.

Mitarbeiter/innen


Forschung
Synthetische Tumor-Immunmikroumgebungen
Zentrale Forschungsfragen
Wie passen sich Krebszellen an ihre Immunmikroumgebung an? Wie beeinflusst die Anwesenheit von Immunzellen in der Umgebung von Krebszellen deren Reaktion auf Therapien?
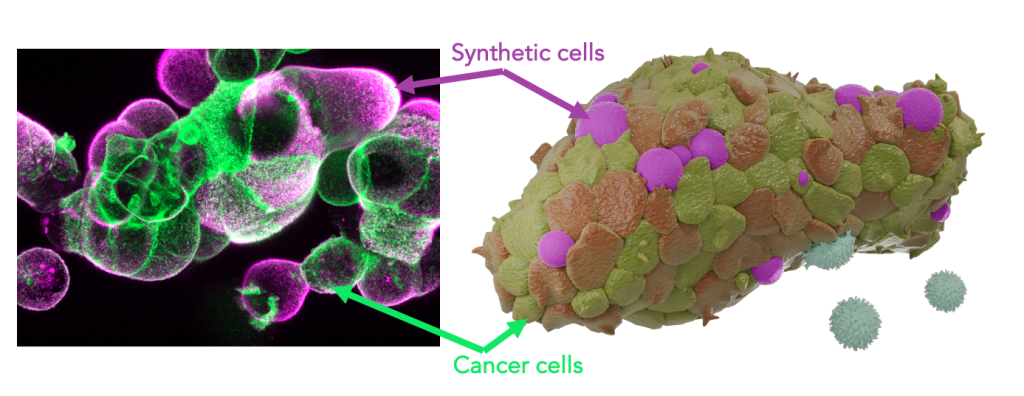
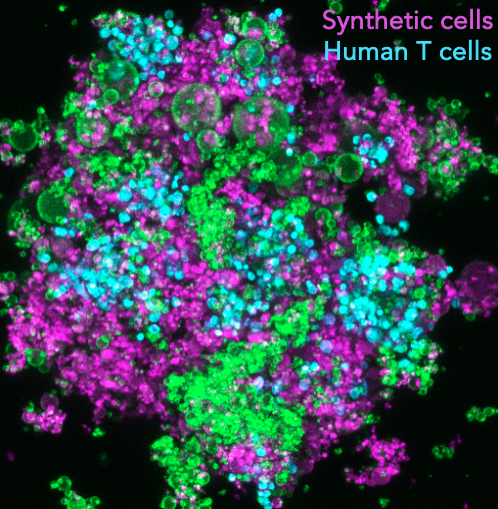
Im Rahmen dieses Projekts entwickeln wir künstliche Tumor-Immunmikroumgebungen (TIME) für humane Pankreaskarzinom-Organoide, um eine strukturierte und rationale Analyse der Immunanpassung von Tumoren zu ermöglichen. Immunzellen, die prägenden Elemente einer Immunmikroumgebung, werden dabei als synthetische Zellen nach dem Bottom-up-Prinzip aus ihren molekularen Bausteinen rekonstruiert. Diese programmierbaren synthetischen Zellen werden in Tumororganoide eingebracht, wo sie als lebensnahe Leukozytenmimetika fungieren und immunologische Effektorfunktionen präsentieren.
Auf diese Weise entsteht eine molekular definierte Immunumgebung innerhalb der Tumormodelle. Multiparametrische Screenings erfassen die Organoidentwicklung sowie die Immuntherapieantwort in Abhängigkeit von der jeweiligen Konfiguration der synthetischen Mikroumgebung. Diese Strategie verknüpft die Architektur von TIMEs mit der Immunanpassung und -umgehung von Krebszellen, um eine quantitative Beschreibung von Therapieresistenzen zu ermöglichen. Das Projekt zielt darauf ab, die dynamische Komplexität der Tumor Immunmikroumgebung rational zu entschlüsseln. Darüber hinaus liefert es neue Konzepte für die Assemblierung hybrider Biomaterialien, die wesentliche Eigenschaften lebender Zellen verkörpern.
Synthetische lymphatische Gewebe
Zentrale Forschungsfragen
Welche mikroanatomischen Architekturen und mechanischen Eigenschaften fördern die T-Zell-Stimulation in Lymphknoten? Wie sammeln und integrieren T-Zellen Signale innerhalb der Lymphknoten? Wie können T-Zellen auf programmierbare, langanhaltende und kontrollierte Weise zu therapeutischen Zwecken aktiviert werden?
T-Zellen spielen eine entscheidende Rolle bei der Bekämpfung von Krankheiten und der Aufrechterhaltung einer langfristigen Immunität. Ihre Reifung ist ein präzise abgestimmter Prozess, der in den Lymphknoten, den zentralen Steuerzentren des Immunsystems, stattfindet. Diese Knoten bestimmen nicht nur, welche spezifischen T-Zell-Typen stimuliert werden, sondern schaffen auch die optimale Umgebung für deren Aktivierung, um eine gezielte und effektive Immunantwort sicherzustellen. Diese Reifung umfasst eine Abfolge von Ereignissen, darunter die initiale Stimulation, die monoklonale Expansion und die Differenzierung. Die Reihenfolge und Dauer dieser Schritte sind entscheidend für die Entwicklung einer vielfältigen T-Zell-Population und einer erfolgreichen adaptiven Immunantwort.
Während der T-Zell-Reifung verändert sich die zelluläre Mikroumgebung innerhalb der Lymphknoten fortlaufend, was zu Änderungen in den biochemischen und biomechanischen Eigenschaften der benachbarten Zellen führt. Solche Veränderungen, etwa eine Zunahme der Gewebesteifigkeit oder die Freisetzung zusätzlicher stimulierender Liganden, steuern die T-Zell-Reifung und fördern ihre Differenzierung. Beispielsweise kommt es während der T-Zell-Expansion in der Lymphknoten-Umgebung zu einer etwa dreifachen Erhöhung der Steifigkeit, und umliegende Zellen setzen vermehrt stimulierende Liganden und Zytokine wie IL-7 und CCL21 frei.
Bestehende in-vitro-Technologien zur T-Zell-Expansion können diese komplexe Abfolge der natürlichen Prozesse bislang jedoch nicht nachbilden. Unser Projekt zielt daher darauf ab, ex-vivo-Expansionsplattformen für T-Zellen zu entwickeln, die diese in-vivo-Prozesse nachahmen und Module zur Anpassung der T-Zell-Mikroumgebung unter Verwendung synthetischer Zellen integrieren. Mit diesem Ansatz wollen wir die Herstellung hochwertiger, therapeutisch wirksamer T-Zellen für die Immuntherapie gezielt verbessern.
Synthetische Tumornischen
Zentrale Forschungsfragen
Wie können sich Leukämiezellen in Lymphknoten verstecken? Welche Überlebens- und Resistenzsignale erhalten sie dort? Wie können wir ex-vivo-Systeme entwickeln, die diese relevanten Prozesse nachbilden und untersuchen?
Leukämie, eine Form von Blutkrebs, stellt nach wie vor eine große Herausforderung in der Onkologie dar. Obwohl viele Patientinnen und Patienten zunächst gut auf Behandlungen ansprechen und moderne Immuntherapien die Prognose deutlich verbessert haben, bleiben Rückfälle ein gravierendes Problem. Ein wesentlicher Grund dafür ist, dass bestimmte Leukämiezellen in den Lymphknoten Zuflucht finden. Unter normalen physiologischen Bedingungen bieten diese Knoten eine nährende Umgebung, in der weiße Blutzellen wachsen und sich vermehren können. Unter pathologischen Bedingungen können sie jedoch unbeabsichtigt zu Schutzräumen für therapieresistente Leukämiezellen werden.
In diesem Projekt wollen wir die zentralen Signale entschlüsseln, die Lymphknoten an ansässige Leukämiezellen senden und ihnen Therapieresistenz verleihen. Dazu konstruieren wir eigene synthetische Lymphknoten nach dem Bottom-up-Prinzip, deren biochemische und biophysikalische Eigenschaften gezielt an jene angepasst werden, die bei Leukämiepatienten beobachtet werden. Anschließende Behandlungen mit Chemotherapie und Antikörper-Immuntherapien ermöglichen es uns, zu untersuchen, inwiefern die Lymphknoten-Umgebung das Überleben von Krebszellen unterstützt. Dieses Vorhaben ist zwar in der Grundlagenforschung verankert, birgt jedoch großes Potenzial, vorhersagende Erkenntnisse für die translationale Medizin zu liefern.

Forschungsphilosophie
- Fundamentale Wissenschaft und technologische Fortschritte im Gleichgewicht: Im Zentrum unserer Arbeit steht ein tiefes Verständnis für die Bedeutung der Grundlagenforschung als Ausgangspunkt technologischer Innovationen. Gleichzeitig erkennen wir an, dass neue Technologien unser grundlegendes Verständnis biologischer Prozesse vertiefen und erweitern können. In dieser symbiotischen Beziehung vereint unser Labor sowohl die fundamentalen als auch die innovativen Aspekte der Lebenswissenschaften
- Synthetische Biologie & „Understanding by Design“: Das bloße Beobachten oder Manipulieren von Molekülen, Zellen und Organismen reicht nicht aus, um die Komplexität biologischer Systeme wirklich zu begreifen. Wir folgen den Prinzipien der synthetischen Biologie und vertreten einen „Understand-by-Design“-Ansatz. Indem wir biologische Systeme aus einer ingenieurwissenschaftlichen Perspektive betrachten, wollen wir quantitative Einsichten gewinnen und unser wissenschaftliches Denken durch neue empirische Evidenz stärken.
- Erkenntnis vor Daten: Obwohl datengetriebene Forschung das Fundament der Wissenschaft bildet, sind es oft die konzeptuellen Einsichten, die den größeren Wert besitzen. Wir glauben an die Kraft von Ideen und betonen die Bedeutung von Argumenten, die auf Experimenten und Mechanismen beruhen, anstatt lediglich Daten anzusammeln.
Über diese Grundpfeiler hinaus legt unser Labor großen Wert auf Zusammenarbeit. Wir fördern eine Umgebung, in der alle, unabhängig von ihrer Karrierestufe, dazu ermutigt werden, Ideen und konstruktive Kritik einzubringen. Offener Dialog ist unsere Stärke: Durch ehrliche und mitunter kontroverse Diskussionen entstehen neue bahnbrechende Erkenntnisse und Konzepte.
Unser übergeordnetes Ziel ist es, ein förderndes Umfeld zu schaffen, in dem Studierende ihr Potenzial entfalten und Wissenschaftlerinnen und Wissenschaftler alles erhalten, was sie brauchen, um neue Perspektiven zu entdecken.
Success stories
Obwohl unser Labor erst vor kurzer Zeit gegründet wurde, gehören wir bereits zur Spitze der Pioniere neuer Konzepte in der Synthetischen Biologie und Immuntherapie. Unsere Beiträge haben schon jetzt nachhaltige wissenschaftliche Wirkung entfaltet.
Beyond the Spike: Bahnbrechende Entdeckungen im Herzen einer Pandemie
Die COVID-19-Pandemie stellte uns alle vor enorme persönliche und wissenschaftliche Herausforderungen. Während Länder weltweit mit Lockdowns kämpften, intensivierten Wissenschaftler:innen ihre Bemühungen, die Geheimnisse des SARS-CoV-2-Virus zu entschlüsseln – auch wir leisteten unseren Beitrag.
Im Sommer 2020, zu Beginn der Pandemie, arbeiteten wir mit einem interdisziplinären Team der University of Bristol und des Max Planck Center Bristol (UK) zusammen. Dort gelang unseren Kolleg:innen eine bahnbrechende Entdeckung: Sie identifizierten die molekulare Struktur des SARS-CoV-2-Spike-Proteins, das unerwartet an eine Fettsäure, nämlich Linolsäure, bindet (Toelzer et al. (2020) Science).
Diese Entdeckung war von großer Bedeutung: Die Fettsäure „verriegelte“ das Spike-Protein und verhinderte so, dass das Virus Zellen infizieren konnte. Uns wurde schnell klar, welch tiefgreifende Konsequenzen dies für das Verständnis von COVID-19 haben könnte.
Mit dem Fortschreiten der Pandemie untersuchten wir die Rolle der Fettsäure-Bindungstasche genauer. Bemerkenswerterweise behielten alle auftretenden Virusvarianten diese Struktur bei. Mithilfe unseres Understand-by-Design-Ansatzes entwickelten wir gemeinsam mit dem Max Planck Center nicht-infektiöse, molekular definierte, minimale synthetische Varianten von SARS-CoV-2-Virionen. Dadurch konnten wir die Rolle der Fettsäure bei der Virus-Zell-Interaktion systematisch analysieren (Staufer et al. (2021) Nature Communications).
Unsere Forschung führte zu einem Modell, das den evolutionären Vorteil der Fettsäure-Bindungstasche erklärt: Sie schützt das Virus vor der Immunerkennung. Dieser molekulare Schalter moduliert die Infektiosität des Virus in Abhängigkeit von der lokalen Aktivität des Immunsystems und Entzündungsprozessen.
Unsere minimalen Virionen trugen zudem dazu bei, die Evolution und Diversität von SARS-CoV-2 besser zu verstehen (Gupta et al. (2021) Nature Communications) ) und gaben Aufschluss darüber, wie das Virus die Bildung immunologischer Synapsen hemmt (Onnis et al. (2022) Journal of Experimental Medicine).
Die Entdeckungen rund um die Fettsäure-Bindungstasche inspirierten schließlich die Gründung von Halo Therapeutics, einem britischen Unternehmen, das heute an Pan-Coronavirus-Therapien arbeitet – und kürzlich erfolgreich seine Series-A-Finanzierungsrunde abgeschlossen hat!
Zusammenfassend war unsere Reise sowohl herausfordernd als auch bereichernd: Wir konnten bahnbrechende wissenschaftliche Entdeckungen machen, spannende Diskussionen führen und neue Partnerschaften aufbauen – alles getragen von unserem Understand-by-Design-Ansatz. Diese Erfahrung belegt eindrucksvoll die Kraft von Zusammenarbeit und Innovation in Zeiten der Krise.
Synthetic Surge: Das Bauprinzip des Lebens im Zeitalter der neuen Biologie
Der Understand-by-Design-Ansatz ist in der Biologie kein neues Konzept. Seit Jahrzehnten versuchen Wissenschaftler:innen, zelluläres Leben nachzubilden. Doch erst mit dem Aufkommen fortgeschrittener molekularer Systemtechnik und der Fähigkeit, supramolekulare Systeme im Reagenzglas zu konstruieren, hat sich das Tempo dieser Entwicklung revolutionär beschleunigt. Heute können wir natürliche Zellen mit unterschiedlichen Funktionen – von der Zellteilung bis zur Immunregulation – gezielt nachahmen.
Mit diesen modernsten Werkzeugen hat weltweit ein Wettlauf um die Erzeugung synthetischer Zellen begonnen. Zahlreiche Labore und Initiativen verfolgen das gemeinsame Ziel, die ersten lebenden synthetischen Zellen zu schaffen. Während einige Gruppen sich auf die Grundlagen des Lebens konzentrieren, sehen andere in diesen kontrollierbaren Systemen Zukunftspotenziale für Nachhaltigkeit und Medizin.
Angeregt durch die SynCell-Konferenz 2021 und in enger Zusammenarbeit mit internationalen Partnern, haben wir es uns zur Aufgabe gemacht, diese weltweiten Bestrebungen zu bündeln. Gemeinsam mit jungen Wissenschaftler:innen aus den USA, Großbritannien, den Niederlanden, Spanien, Deutschland, Frankreich, Japan und Australien haben wir Strategien entwickelt, um die nächste Generation von Innovator:innen für dieses Forschungsfeld zu begeistern.
Unser Ziel geht über die bloße Erzeugung von Zellen hinaus: Wir möchten eine globale Community aufbauen, die synthetische Zellen und Organellen von Grund auf konstruiert! Wir haben Wege aufgezeigt, um die sozioökonomischen und technologischen Auswirkungen synthetischer Zellen zu verstärken, und betont, wie wichtig eine vernetzte, interdisziplinäre Forschungslandschaft ist (Staufer et al. (2021) eLife).
Durch den Austausch von Wissen und Ressourcen sowie die Initiierung von Bildungsprogrammen setzen wir uns für eine nachhaltige Zukunft dieses Forschungsfelds ein.
Unsere Reise, die Kontinente und Disziplinen verbindet, ist ein Zeugnis des kollaborativen Geistes der Wissenschaft. Die Leidenschaft und der Enthusiasmus der jungen Forscher:innen, die wir dabei erleben durften, sind eine große Inspiration – und ein eindrucksvoller Beweis dafür, wie lebendig und zukunftsweisend die synthetische Biologie heute ist.
Open position
We pride ourselves on being a diverse team, both culturally and scientifically. Our expertise spans a wide range of the natural sciences, including biophysics, immunology, advanced microscopy, microfluidics, nanotechnology, drug delivery, immunotherapy, virology, molecular biology, membranes, electrophysiology, cell biology, physical chemistry, and more. We invite you to reach out and become a part of our vibrant community.
Postdoctoral Researchers: We have fully-funded postdoc positions available. If you’re considering fellowships, we provide guidance and support for applications, including but not limited to the Marie Curie Fellowship, DFG Walter Benjamin Program, and the Feodor Lynen Fellowship by the Humboldt Foundation. We value your unique research ideas for other programs and offer constructive discussions within our group to help you craft a successful proposal. For postdoc opportunities, please get in touch by sending your interest statement to us directly.
PhD Candidates: We invite applications for our fully funded PhD positions. Our research projects are co-defined with students, emphasizing interdisciplinary training and state-of-the-art methods spanning biophysics, microfluidics, immunology, advanced microscopy, and 3D cell culturing. Send us your motivation letter and CV. We’re eager to hear about your research ideas and welcome you to explore them in our lab.
Master’s Students: We offer opportunities for master’s thesis projects in areas like synthetic cells, immunotherapy, organoids, and biomaterials. While these subjects have a predefined framework, we encourage students to add their unique perspective. Every master’s student is mentored directly by an experienced PhD candidate or postdoc.
High School Students: Unsure about your academic path? Curious about the dynamics of a research lab? We offer short-term research internships, providing a glimpse into the world of natural sciences. Join us and get a hands-on experience.
Publikationen

Burgstaller, Anna | Nink, Tamara | Walter, Niklas | Lopez Lopez, Erick Angel | Chang, Shin-Fang | Staufer, Oskar
DOI:
Synthetic cells have emerged as a novel biomimetic approach for studying fundamental cellular functions and enabling new therapeutic interventions. However, the potential to program synthetic cells into self-organized 3D collectives to replicate the structure and function of tissues has remained largely untapped. Here, self-assembly properties are engineered into synthetic cells to form millimeter-sized 3D lymphatic bottom-up tissues (lymphBUTs) with mechanical adaptability, metabolic activity, and hierarchical microstructural organization. It is demonstrated that primary human immune cells spontaneously infiltrate and functionally integrate into these synthetic lymph nodes to form living tissue hybrids. Applying lymphBUTs, it is shown that structured 3D organization and mechanical support drives T cell activation and the application of lymphBUTs for ex vivo expansion of regulatory CD8+ T cells is demonstrated. The study highlights the functional integration of living and non-living matter, advancing synthetic cell engineering toward 3D tissue structures.
Balabanov, Ivaylo | Madureira, Sara | Burgstaller, Anna | Fehlberg, Maja | Piernitzki, Nils | Abdukarimov, Nurzhan | Lautenschlaeger, Franziska | Staufer, Oskar
DOI:
Hematopoietic stem cells (HSCs) receive a combination of biochemical and biomechanical signals within the bone marrow that guide their differentiation process. These include soluble factor signaling with cytokines, cellular confinement in the stem cell niche, and contact-dependent receptor–ligand interactions with stromal cells. Recreating this complex microenvironment in vitro is a principal engineering challenge for regenerative therapies and tissue engineering. While cytokines can be easily supplemented in vitro, and several systems for confined HSC culture have been developed, integrating receptor-based intercellular interactions found in stem cell niches has only been achieved with quantitatively undefined heterotypic co-cultures. We report here the development of microwell-based systems that integrate synthetic cells to mimic receptor–ligand interactions within hematopoietic niches. The synthetic cells are based on droplet-supported lipid bilayers (dsLBs) with cytomimetic stiffness and present Notch receptor ligands on a laterally mobile lipid membrane. We show the system's applicability to individually tune the three signaling axes: soluble factors, confinement, and intercellular interactions for HSC differentiation. Introducing synthetic cells as an alternative to coculture and feeder cells opens the possibility to engineer precisely defined HSC niches with adjustable biochemical and biomechanical properties.
Yandrapalli, Naresh | Gonazles, David T. | Leng, Weihua | Alsayyah, Cynthia | Abdukarimov, Nurzhan | Ernst, Robert | Dora Tang, T.-Y.
DOI:
Lipid vesicles are important as minimal model systems for cellular compartmentalization. They drive major advances in deciphering biological mechanisms by molecular reconstitution; provide rational solutions for primitive compartmentalization in origin-of-life studies; form the basis of synthetic cells and drug delivery vehicles. The emulsion method is a well-established route for producing bilayer lipid vesicles. However, the application of this method in microfluidics requires complex and specialized machinery. The bulk method suffers from the need to physically manipulate the vesicles through oil layers for characterization that can damage the vesicles. Given this, we present a facile and robust method for on-chip production and manipulation of lipid vesicles by the emulsion method. We prepared a simple device that allows preparation, imaging, and collection of activated lipid vesicles. This technique combines minimal processing steps with maximum flexibility in lipid vesicle production and manipulation with direct imaging, thus fast-tracking production lines across disciplines.
Zhou, Xiangda | Zhang, Sijia | Yang, Wenjuan | Gonder, Susanne | Sadjadi, Zeinab | Piernitzki, Nils | Moter, Alina | Sharma, Shulagna | Largeot, Anne | Küchler, Nadja | Kaschek, Lea | Schäfer, Gertrud | Schwarz, Eva C. | Eichler, Hermann | Ullrich, Evelyn | Rieger, Heiko | Staufer, Oskar | Paggetti, Jérome | Moussay, Etienne | Hoth, Markus | Qu, Bin
DOI:
Natural killer (NK) cells are critical components of the first-line immune defense, responsible for eliminating tumorigenic cells. NK cell-based adoptive immunotherapy has gained increasing attention; however, cryopreservation, a standard technique for NK cell storage, significantly impairs NK cell cytotoxicity, particularly in physiological 3D environments. Here, we demonstrate that short-term co-culture with effector T cells markedly enhances NK cell motility and killing functionality. Notably, a brief 1-day co-culture is sufficient to restore cryopreservation-impaired NK cell functionality in 3D environments. This enhancement requires direct contact between T cells and NK cells, which facilitates localized high concentrations of IL-2 at the cell contact sites. To develop a controled, donor-independent solution, we demonstrate that synthetic T cells with surface-bound IL-2 exhibit superior efficiency in revitalizing cryopreserved NK cells. These findings uncover a previously unrecognized role for physical contact-mediated local IL-2 signaling and provide an efficient, cost-effective, and tunable strategy to rescue NK cell functionality post-cryopreservation, paving the way for more scalable, potent, and clinically viable NK cell-based immunotherapies.
Leithner, Alexander | Staufer, Oskar | Mitra, Tanmay | Liberta, Falk | Valvo, Salvatore | Kutuzov, Mikhail | Dada, Hannah | Spaeth, Jacob | Zhou, Weijie | Schiele, Felix | Reindl, Sophia | Nar, Herbert | Hoerer, Stefan | Crames, Maureen | Comeau, Stephen | Young, David | Low, Sarah | Jenkins, Edward | Davis, Simon J. | Klenerman, David | Nixon, Andrew | Pefaur, Noah | Wyatt, David | Dushek, Omer | Kasturirangan, Srinath | Dustin, Michael L.
DOI:
Bispecific T cell engagers (TcEs) link T cell receptors to tumor-associated antigens on cancer cells, forming cytotoxic immunological synapses (IS). Close membrane-to-membrane contact (≤13 nm) has been proposed as a key mechanism of TcE function. To investigate this and identify potential additional mechanisms, we compared four immunoglobulin G1-based (IgG1) TcE Formats (A–D) targeting CD3ε and Her2, designed to create varying intermembrane distances (A < B < C < D). Small-angle X-ray scattering (SAXS) and modeling of the conformational states of isolated TcEs and TcE–antigen complexes predicted close contacts (≤13 nm) for Formats A and B and far contacts (≥18 nm) for Formats C and D. In supported lipid bilayer (SLB) model interfaces, Formats A and B recruited, whereas Formats C and D repelled, CD2–CD58 interactions. Formats A and B also excluded bulky Quantum dots more effectively. SAXS also revealed that TcE–antigen complexes formed by Formats A and C were less flexible than complexes formed by Formats B and D. Functional data with Her2-expressing tumor cells showed cytotoxicity, surface marker expression, and cytokine release following the order A > B = C > D. In a minimal system for IS formation on SLBs, TcE performance followed the trend A = B = C > D. Addition of close contact requiring CD58 costimulation revealed phospholipase C-γ activation matching cytotoxicity with A > B = C > D. Our findings suggest that when adhesion is equivalent, TcE potency is determined by two parameters: contact distance and flexibility. Both the close/far-contact formation axis and the low/ high flexibility axis significantly impact TcE potency, explaining the similar potency of Format B (close contact/high flexibility) and C (far contact/low flexibility). Copyright © 2025 the Author(s).
Burgstaller, Anna | Madureira, Sara | Staufer, Oskar
DOI:
Tissue functions rely on complex structural, biochemical, and biomechanical cues that guide cellular behavior and organization. Synthetic cells, a promising new class of biomaterials, hold significant potential for mimicking these tissue properties using simplified, nonliving building blocks. Advanced synthetic cell models have already shown utility in biotechnology and immunology, including applications in cancer targeting and antigen presentation. Recent bottom-up approaches have also enabled synthetic cells to assemble into 3D structures with controlled intercellular interactions, creating tissue-like architectures. Despite these advancements, challenges remain in replicating multicellular behaviors and dynamic mechanical environments. Here, we review recent advancements in synthetic cell-based tissue formation and introduce a three-pillar framework to streamline the development of synthetic tissues. This approach, focusing on synthetic extracellular matrix integration, synthetic cell self-organization, and adaptive biomechanics, could enable scalable synthetic tissues engineering for regenerative medicine and drug development.
Piernitzki, Nils | Gao, Ning | Gasparoni, Gilles | Krauß, Louisa M. | Schulze-Hentrisch, Julia | Dustin, Michael | Schrul, Bianca | Györffy, Balázs | Mann, Stephen | Staufer, Oskar
DOI:
Self-assembly is a fundamental property of living matter that drives the three-dimensional organization of cell collectives such as tissues and organs. Here, the co-assembly of synthetic and natural cells is leveraged to create hybrid living 3D cancer cultures. We screen a range of synthetic cell models for their ability to form augmented tumoroids with artificial but controllable micro-environments, and show that the balance of inter- and extracellular adhesion and synthetic cell surface tension are key material properties driving integrated co-assembly. We demonstrate that synthetic cells based on droplet-supported lipid bilayers can establish artificial tumor immune microenvironments (ART-TIMEs), mimicking immunogenic signals within tumoroids and eliminating the need to integrate complex living immune cells. Using the ART-TIME approach, we identify a AhR-ARNT-mediated co-signaling mechanism between PD-1 and CD2 as a driver in immune evasion of pancreatic ductal adenocarcinoma. Our study advances the field of hybrid organoid engineering, offers opportunities for the construction and modelling of artificial tumour environments, and marks a step towards the design of functional living/non-living cytomimetic materials.
Piernitzki, Nils | Staufer, Oskar
DOI:
Extracellular vesicles (EVs) are lipid-membrane-enclosed particles released from cells, playing a pivotal role in cellular communication, particularly within the immune system. The fundamental molecular mechanisms through which EVs offer unique functionality for immunotherapeutic benefits are identified and reviewed. The focus is on three essential features, all rooted in the EV lipid membrane: immune receptor–ligand interactions at the EV membrane interface, the shielding of immunogenic cargo within the EVs, and the fusion of EVs with target cell membranes for direct cargo delivery. From this, how these distinct EV attributes, from their initial description and analysis in immune communication, have led to the development of novel immunotherapeutic strategies is traced. This review delves into how these strategies are applied in various immunotherapies, such as cancer immunotherapy, autoimmune diseases, infections, vaccinations, and graft-versus-host diseases, to modulate communication among different cell types for immune regulation. It is concluded by reviewing clinical trials involving EVs in immunotherapy that have effectively harnessed EVs' unique molecular mechanisms in clinical settings. Research and standardization efforts to maximize the potential impact of EVs on immunotherapy are further suggested.
DOI:
In a major advancement for synthetic biology, dynamin A has been identified as a minimal component enabling cell division in synthetic cells, moving us one step nearer to realizing the ambition of creating synthetic life forms.
Jahnke, Kevin | Staufer, Oskar
DOI:
Extracellular vesicles (EVs), lipid-enclosed structures released by virtually all life forms, have gained significant attention due to their role in intercellular and interorganismal communication. Despite their recognized importance in disease processes and therapeutic applications, fundamental questions about their primary function remain. Here, we propose a different perspective on the primary function of EVs, arguing that they serve as essential elements providing membrane area for long-distance, contact-dependent cellular communication based on protein-protein interaction. While EVs have been recognized as carriers of genetic information, additional unique advantages that they could provide for cellular communication remain unclear. Here, we introduce the concept that the substantial membrane area provided by EVs allows for membrane contact-dependent interactions that could be central to their function. This membrane area enables the lateral diffusion and sorting of membrane ligands like proteins, polysaccharides or lipids in two dimensions, promoting avidity-driven effects and assembly of co-stimulatory architectures at the EV-cell interface. The concept of vesicle-induced receptor sequestration (VIRS), for example, describes how EVs confine and focus receptors at the EV contact site, promoting a dense local concentration of receptors into signalosomes. This process can increase the signalling strength of EV-presented ligands by 10-1000-fold compared to their soluble counterparts. The speculations in this perspective advance our understanding of EV-biology and have critical implications for EV-based applications and therapeutics. We suggest a shift in perspective from viewing EVs merely as transporters of relevant nucleic acids and proteins to considering their unique biophysical properties as presentation platforms for long-distance, contact-dependent signalling. We therefore highlight the functional role of the EV membrane rather than their content. We further discuss how this signalling mechanism might be exploited by virus-transformed or cancer cells to enhance immune-evasive mechanisms.




